动态信息
中国农业科学院兰州畜牧与兽药研究所左二伟团队联合多家单位建立首个RNA引导核酸酶多维性能评估框架
近日,中国农业科学院兰州畜牧与兽药研究所左二伟研究员团队联合中国科学院上海药物研究所、华东师范大学、中国科学院动物研究所及北京大学等单位,在国际权威期刊Science Bulletin在线发表了题为“Large-scale parallel characterization of RNA-guided nuclease activity and specificity”的研究论文。该研究首次系统评估了代表性的RNA引导核酸酶的编辑效率、脱靶效应、基因组结构影响及细胞毒性,建立了首个针对该类核酸酶的多维性能评估框架,为精准基因编辑工具的选择与优化提供了重要数据支撑。
随着基因编辑技术的快速发展,新型RNA引导核酸酶不断涌现,但针对其编辑效率、特异性及安全性的系统性比较研究相对滞后,限制了其在基础研究和临床治疗中的精准应用。为填补这一空白,研究团队对涵盖Cas12a、Cas12b、Cas12f、TnpB、Fanzor等10个亚型的50种核酸酶进行了大规模平行评估。结果显示,AsCas12a-Ultra、LbCpf1、AsCas12a-Plus等核酸酶的编辑效率与经典SpCas9相当甚至更高,而紧凑型核酸酶enOsCas12f1在保持较高编辑活性的同时,其小分子尺寸更适于体内递送。在特异性方面,AsCpf1-YH和FnCpf1表现出较低的sgRNA依赖性脱靶风险,而DpFNuc则具有最高的脱靶倾向。此外,研究还发现部分高活性核酸酶(如enCas12f-HKRA)易引发染色体易位,而Cas12j-SF05则具有较低的基因组结构变异风险。在细胞毒性方面,enRhCas12f1和SpaCas12f1对细胞增殖影响最小,而enAsCpf1-HF则显著抑制细胞活力。
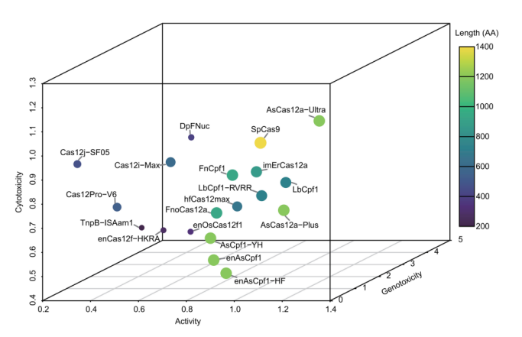
该研究通过整合编辑效率、基因毒性与细胞毒性三个维度,构建了核酸酶性能的三维评估体系,揭示了不同核酸酶在效率与安全性之间的权衡关系,为科研和临床应用场景下的工具选择提供了数据驱动的决策依据。研究还发现,核酸酶的编辑效率与脱靶频率之间无明显相关性,提示二者可独立优化,为后续酶工程改造指明了方向。
需要指出的是,本研究仍存在一定局限性。首先,所有实验均在HEK293T细胞系中进行,其结果在原代细胞、干细胞或体内组织中的可推广性尚需进一步验证。其次,为便于横向比较而采用的统一实验条件,可能因不同编辑器在PAM偏好性及最佳靶向序列上的差异,导致部分工具的真实性能被低估。此外,研究主要关注脱靶效应、染色体易位和短期细胞毒性,而非特异性DNA损伤、长期细胞功能影响及免疫反应等复杂安全性问题尚未系统评估。最后,编辑效率测量依赖于流式细胞术富集转染成功细胞,与体内实际应用场景中的编辑水平存在差异,且细胞毒性机制解析较浅,缺乏动物模型层面的验证。上述局限性提示,将本研究的评估框架拓展至更多生理及病理背景,将是未来研究的重要方向。
中国农业科学院兰州畜牧与兽药研究所左二伟研究员为论文通讯作者,郑基坛、王雪岩、吴明第、刘敬四位博士生与博士后冯虎为共同第一作者。中国科学院上海药物研究所杨辉研究员、华东师范大学李大力教授、中国科学院动物研究所王皓毅研究员、北京大学胡家志教授共同参与研究设计与指导。本研究获深圳市医学研究专项资金、国家自然科学基金、江苏省种业振兴工程、中国农业科学院科技创新工程等项目支持。
https://doi.org/10.1016/j.scib.2026.03.047